Семинар: Плазменные технологии, как они работают
10:00 — 11:30 Плазменные технологии, как они работают. Практические аспекты применения аппарата последнего поколения генерации «холодной» и «горячей» плазмы Plasma BT- показания.
— протоколы, схема лечения
— результаты
— осложнения, реабилитация
12:00 — 14-00: мастер-класс применения аппарата Plasma BT
Докладчик: Лоран Мария Сергеевна — врач-косметолог, сертифицированный тренер компании Seoulin Medi Care (Корея).
Место проведения: Бьюти клуб «Белый Пион» м.Римская\Площадь Ильича, ул. Бульвар Энтузиастов, д.2 бизнес центр «Голден Гейт»
Тел. для записи: 8 (495) 921 40 32


Шептий Олег Васильевич
К.м.н., специалист в области лазерной дерматологии и хирургии, член Американского общества лазерной медицины и хирургии (ASLMS), член Общества специалистов в области фотомедицины, Москва
Генералова Таиса Витальевна
Врач-косметолог центра аппаратной косметологии «Вирсавия», Москва
Использование плазменных технологий является относительно новым направлением в косметологии и пока еще не совсем понятным. Первые устройства создавались как альтернатива лазерному омоложению, однако последние исследования показывают, что возможности использования плазмы гораздо шире.
Плазма: что это такое?
Чтобы понять, какие преимущества дает использование плазменных технологий, давайте сначала разберемся, что такое плазма. Плазма — это газ, который, в отличие от привычных нам стабильных газов, состоит не только из нейтральных молекул, но включает также заряженные частицы — свободные электроны и положительные и отрицательные ионы (а в некоторых случаях состоит только из этих заряженных частиц).
Несмотря на то, что в плазме присутствуют частицы разного знака, количество носителей положительного и отрицательного заряда в единице ее объема практически одинаково — то есть общий заряд плазмы равен нулю. Эта особенность, ставящая плазму особняком от других систем, содержащих заряженные частицы (например, электронные или ионные пучки), получила название квазинейтральность. При этом плазма сохраняет главное свойство, отличающее ее от стабильных газов, — способность взаимодействовать с внешним электромагнитным полем и проводить электрический ток.
В состояние плазмы газ переходит при передаче ему большого количества энергии, которая сможет «оторвать» электроны от атомов. Таким образом, плазму называют четвертым (после твердого, жидкого и газообразного) агрегатным состоянием вещества (рис. 1).
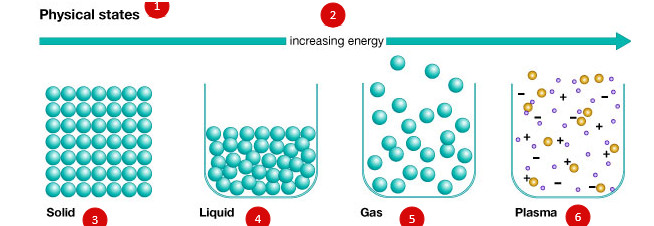
1. Физические состояния вещества
2. Увеличение энергии
3. Твердое вещество. В твердом состоянии вещество сохраняет форму и объем — молекулы, которые его образуют, соединены между собой крепкими связями и расположены строго упорядоченным образом. При низких температурах все вещества замерзают и превращаются в твердые тела
4. Жидкость. В жидком состоянии вещество сохраняет объем, но не сохраняет форму — между молекулами существует притяжение, достаточно сильное, чтобы удержать их на близком расстоянии, но недостаточное для поддержания постоянной структуры.
5. Газ. Молекулы газа взаимодействуют слабо и движутся хаотически, в связи с чем газ заполняет весь доступный объем.
6. Плазма. Является частично или полностью ионизированным газом. Взаимодействует с другими заряженными частицами и электромагнитным полем.
Энергия, которая на это потребуется, зависит от конкретного вещества, а именно строения внешних электронных оболочек его атомов: чем легче атом отдает электрон, тем меньше энергии необходимо затратить на его отрыв. В естественных условиях источником такой энергии является преимущественно нагревание, однако плазму можно получить и иными способами [1].
Различают 2 вида плазмы [2]:
- высокотемпературную — практически полностью ионизованная плазма. Такой вид плазмы присутствует на Солнце, образуется при разряде молний и в ходе термоядерного синтеза. Высокотемпературная плазма считается «классическим» четвертым агрегатным состоянием вещества;
- низкотемпературную — с малой степенью ионизации (до 1%). Обычно ее получают при воздействии на газ электрического тока, ускоряющего электроны, которые в свою очередь ионизируют атомы. Именно с таким типом плазмы работают технологические производства и медицина.
Биомедицинские эффекты плазмы
Плазма является источником [2]:
- тепла;
- реактивных форм кислорода, азота и свободных радикалов;
- различных видов излучения (от ультрафиолетового до инфракрасного).
Конкретные эффекты при взаимодействии с тканями-мишенями будут зависеть от типа применяемой плазмы, ее дозы, скорости потока, давления, времени воздействия (параметры, которые на которые можно влиять с помощью модификации устройств) и характеристик самой ткани [3].
Первоначально медицина взяла на вооружение тепловые эффекты плазмы. Так, высокоскоростной поток плазмы, получаемый с помощью воздействия на инертные газы электрического тока большой силы, известен как плазменный нож и используется для рассечения и удаления тканей. Способность плазмы нагревать ткани (хотя уже с меньшей интенсивностью) стало фундаментом ее использования и в косметологии [4].
Однако нужно сказать, что в последние годы все больше внимания привлекает к себе технология холодной низкотемпературной плазмы (35–40оС), которая позволяет добиваться лечебных эффектов без повреждения живых тканей.
В настоящее время изучается возможность применения способности холодной низкотемпературной плазмы генерировать свободные радикалы и ультрафиолетовое излучение для дезинфекции кожи человека, а также для обработки ран. Такое воздействие позволяет убить устойчивые к антибиотикам микроорганизмы (что особенно актуально для внутрибольничных инфекций), не повреждая при этом саму кожу. Противомикробная активность плазмы была продемонстрирована не только на лабораторных животных, но и в ходе рандомизированных контролируемых исследований на людях: двухминутная обработка ран с помощью холодной аргоновой плазмы обуславливала значительное уменьшение количества как грамотрицательных, так и грамположительных бактерий в ранах [5].
Кроме того, было выявлено, что обработка ран холодной низкотемпературной плазмой ускоряет их заживление [6]. Недавняя работа, опубликованная в журнале Scientific Reports, продемонстрировала, что такая плазма стимулирует пролиферацию и дифференцировку кератиноцитов за счет активации β-катенин-сигнального пути и ингибирования Е-кадгерина, который отвечает за контактное торможение клеточного роста. У мышей, раны которых обрабатывались низкотемпературной плазмой, уже спустя 15 дней отмечалось практически полное восстановление эпидермиса и мышечной ткани, а также высокая плотность коллагеновых волокон, в то время как в ранах, заживающих естественным образом, эти процессы шли гораздо медленнее (рис. 2) [7].
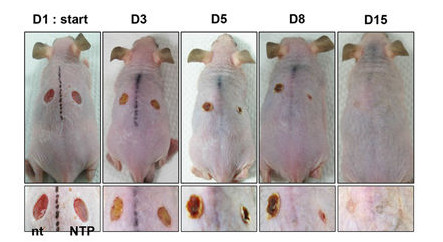
Рана слева заживала естественным образом, рана справа 3 раза в день в течение 5 мин обрабатывалась холодной низкотемпературной плазмой на протяжении 2 нед [7]
Последние исследования также выявили, что холодная плазма обуславливает временное снижение барьерной функции рогового слоя и усиливает проницаемость кожи для лекарственных и косметических средств. Предполагается, что это связано с перестройкой липидных бислоев под действием плазмы и формированием временных каналов, облегчающим прохождение различных веществ (рис. 3) [9].
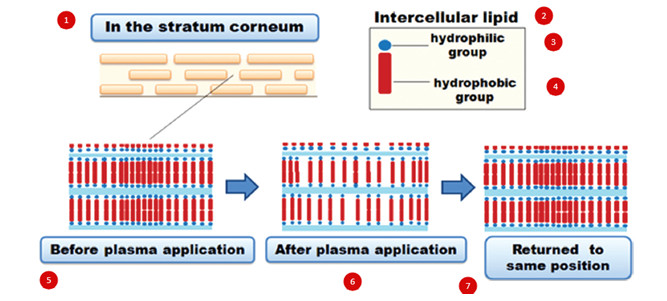
1. Роговой слой
2. Межклеточные липиды
3. Гидрофильная группа
4. Гидрофобная группа
5. До обработки плазмой
6. После плазменного воздействия
7. Возвращение к исходному состоянию
Также продемонстрировано, что импульсные электрические поля, формирующиеся при контакте плазмы с кожей, способны изменять электрический заряд клеточных мембран и образовывать поры, через которые в клетку могут поступать различные активные вещества. Это явление известно как электропорация [10].
Кроме того, плазма влияет на свертываемость крови, иммунную систему, а также пролиферацию и апоптоз раковых клеток [10].
Плазменные методы в косметологии
Начало эры плазменных технологий в косметологии связано с тепловыми эффектами плазмы. Так, плазменные методы омоложения основаны на контролируемом термическом повреждении тканей с целью запуска регенеративных процессов и «обновления» тканей. Этот принцип является основной и других методов аппаратного омоложения, однако в случае использования плазмы есть свои особенности.
Плазменная регенерация кожи
Пионером плазменного омоложения является технология плазменной регенерации кожи (Plasma Skin Regeneration, PSR), которая появилась в 2006 г., а первым устройством стал Portrait PSR (Rhytec, Великобритания). В качестве плазмообразующего газа было предложено использовать азот — инертный газ, который способен вытеснять кислород, необходимый для окисления и горения, с поверхности кожи, и таким образом минимизировать риск ожога и образования рубцов.
Под действием ультравысокочастотного электрического тока в рукоятке устройства происходит ионизация молекул азота и образуется плазма, которая доставляется к коже бесконтактным способом в виде миллисекундных импульсов (такой бесконтактный способ обработки позволяет коже быстро остывать и исключает риск ожогов от деталей устройства). То есть, по сути, плазма является «переносчиком» электрической энергии.
Как только плазма попадает на кожу, ее энергия быстро распределяется по поверхности и обеспечивает градиентный нагрев кожи — сначала эпидермиса, а затем (в зависимости от используемого уровня энергии) дермы с формированием поверхностной зоны необратимого термического повреждения и более глубокой зоны термической модификации (рис. 4) [11].
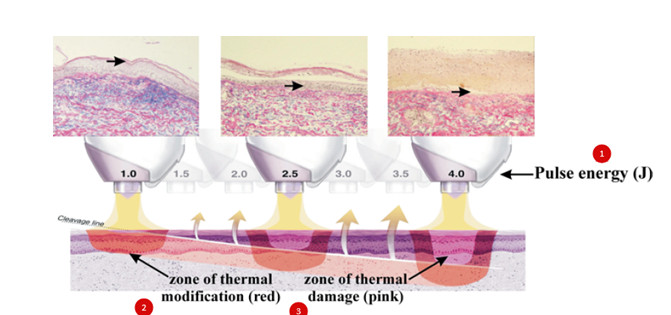
1. Энергия импульса
2. Зона термической модификации (красная)
3. Зона термического повреждения (розовая)
Глубина и площадь теплового эффекта определяются установкой энергии и размером пятна наконечника, которое можно увеличить или уменьшить, приближая или удаляя наконечник от поверхности кожи. Так, низкоэнергетические импульсы (около 1 Дж) оказывают воздействие только на эпидермис, а высокоэнергетические (3–4 Дж) обеспечивают нагревание дермы (глубина достигает 500–600 мкм) [11].
Важно, что, в отличие от лазеров, плазма не требует наличия хромофоров в коже, поэтому разогрев тканей протекает равномерно, без «взрывной» вапоризации тканей. Слой старого поврежденного эпидермиса служит «биологической защитной повязкой» нижележащим клеткам и остается на месте, пока не образуется новый, а затем постепенно отшелушивается. Кроме того, это позволяет проводить обработку кожи любых фототипов и сокращает риск побочных эффектов в виде шрамов, инфекций и депигментации. Даже в случае высокоэнергетического воздействия неоэпителизация происходит быстро и обычно завершается в течение 5–7 дней после процедуры.
Процессы, протекающие в дермальном слое, более длительные. Сразу после обработки отмечается контракция коллагеновых волокон (в тех областях, где температура нагревания превышала 60оС) и реакции на тепловой шок, затем происходит постепенное разрушение поврежденных структур и активация неоколлагенеза и неоэластогенеза. Процессы ремоделирования дермы продолжаются как минимум 3 мес после обработки [11–13].
- Низкоэнергетическая обработка дает поверхностное воздействие по типу легкого пилинга и обеспечивает осветление и выравнивание тона кожи и мелких морщин (рис. 5) [11]. Курс состоит из 3–4 процедур с перерывом в 3 нед и не требует реабилитации.
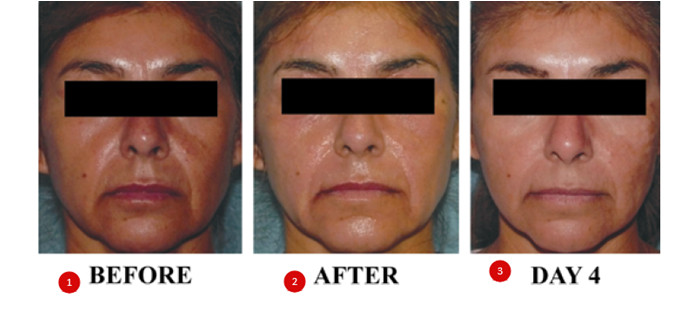
1. До
2. После
3. День 4
- Процедуры с использованием высоких энергий применяются для коррекции морщин, повышения упругости и подтяжки кожи (в том числе кожи верхних и нижних век), уменьшения рубцов и растяжек. Они более дискомфортны и сопровождаются восстановительным периодом в 1–2 нед (рис. 6) [11].
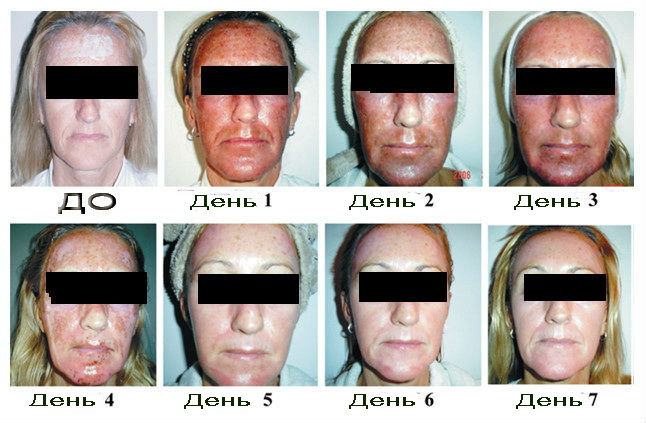
Фракционная микроплазменная RF-технология
Еще одним вариантом использования особых свойств плазмы для проведения омолаживающих процедур является фракционная микроплазменная RF-технология, появившаяся в 2010 г. и реализованная в устройстве Pixel RF (Израиль).
На специальных наконечниках манипулы (в виде подвижных роликов или плоских стационарных насадок) размещено множество игольчатых электродов (спикул). При приближении к поверхности кожи на несколько микрометров мощный электрический радиочастотный разряд, проходящий через электроды, формирует вспышки плазмы (микроплазменные разряды высокой плотности).
Эти вспышки «пробивают» эпидермис и верхние слои дермы, образуя микроканалы, окруженные зоной термического повреждения. При дальнейшем вращении роллера (или надавливании стационарной насадкой) спикулы вдавливаются в эти участки абляции, оказывая на них дополнительное механическое воздействие.
Глубина и размеры повреждений также будут определяться энергией и продолжительностью импульсов (согласно исследованиям на коже поросят, колодцы абляции могут достигать 50–200 мкм в глубину и 80–200 мкм в диаметре, а зона коагуляции — распространяться еще на 100–200 мкм вокруг них). Эпителизация завершается через 3–4 дня, процессы ремоделирования дермы длятся вплоть до 6 мес [14].
Фракционная микроплазменная RF-обработка рекомендуется для коррекции возрастных изменений (морщин, дряблости кожи и т.д.), а также для выравнивания тона кожи и уменьшения рубцов. Кроме того, быстрота выполнения процедур (в среднем 10 мин для 5 проходов по лицу) позволяет использовать роллеры для обработки больших площадей кожи, например, живота.
Плазма vs. лазеры
Каковы же особенности плазменного омоложения по сравнению с лазерным, альтернативой которому оно изначально создавалось?
В отличие от лазеров, плазму можно использовать на коже любых фототипов. Гиперпигментация, которая может встречаться после процедур, в целом возникает реже, чем в случае лазерной обработки. Также существенно снижен риск инфицирования и рубцевания.
Продемонстрировано, что СО2-лазеры формируют более однородные по глубине и диаметру повреждения, в то время как в случае использования плазмы эти размеры могут варьировать. Кроме того, лазеры обеспечивают более глубокое воздействие, чем плазма. Однако именно более поверхностные эффекты плазменной обработки могут быть одной из причин меньшего риска поствоспалительной гиперпигментации [14].
Что касается эффективности процедур, то было проведено непосредственное сравнение фракционной микроплазменной RF-технологии и фракционного СО2-лазера для устранения рубцов постакне. Одна сторона лица пациентов (всего участвовало 33 человека с III и IV фототипами кожи) обрабатывалась с помощью плазмы, другая — лазера, по 3 процедуры каждого вида. Глубина повреждений в первом случае варьировала в пределах 120–150 мкм, а диаметр составлял 150–180 мкм. Фракционный СО2-лазер формировал повреждения глубиной 300–400 мкм и диаметром 100–120 мкм. Зона термического повреждения вокруг колодца абляции была шире в случае микроплазмы (рис. 7).
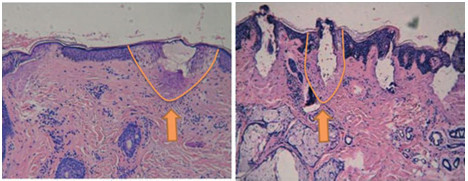
Рис. 7. Гистологические изменения сразу после обработки атрофических рубцов постакне с помощью микроплазменной RF-технологии (слева) и фракционного СО2-лазера (справа)
Оба метода существенно и практически равнозначно снизили выраженность рубцов постакне — с 51,1 ± 14,2 до 22,3 ± 8,6 в случае плазмы (улучшение на 56,4%) и с 48,8 ± 15,1 до 19,9 ± 7,9 для СО2-лазера (улучшение на 59,2%) по шкале ЕССА. При этом в ответ на лазерное воздействие у 12 человек (36,4%) развилась поствоспалительная гиперпигментация, а со стороны микроплазменной обработки таких осложнений зафиксировано не было [15].
Таким образом, низкоэнергентическая плазма позволяет бороться с пигментацией, выравнивать текстуру и тон кожи и, по сути, приравнивается к неаблятивным лазерам. Высокоэнергетическая плазма, в свою очередь, помогает бороться с более серьезными дефектами, как то морщины, снижение эластичности и упругости кожи, а также рубцы постакне и растяжки, однако глубина воздействия будет ограничена верхними слоями дермы (в случае лазеров глубина микротермальных лечебных зон может составлять больше 1 мм).
И хотя плазменное омоложение несет меньший риск побочных эффектов и требует на восстановление меньше времени, эффективность аблятивных лазеров пока остается более высокой. Однако эти процедуры могут быть процедурами выбора у пациентов с темными типами кожи, поскольку для них существенно снижен риск поствопалительной гиперпигментации.
Кроме того, технологии использования плазмы развиваются, и уже сейчас появляется все большее число перспективных устройств с новыми свойствами, которые позволяют им уйти от сравнения с «младшим братом» лазеров и занять отдельную нишу.
Современный рынок плазменных технологий
Основным отличием серьезных профессиональных плазменных аппаратов от портативных устройств для домашнего и салонного использования является наличие контроля над глубиной и степенью повреждения кожи. Это крайне важный аспект, позволяющий получать прогнозируемый результат и снизить риски нежелательных побочных явлений.
Количество новых устройств, использующих возможности плазмы, увеличивается с каждым годом. Появляются даже портативные приборы, позволяющие использовать энергию плазмы в салонных и домашних условиях. Однако нужно отметить, что в них установлены режимы воздействия, в которых нет возможности менять ни силу, ни глубину, ни время обработки, что вызывает вопросы в отношении их эффективности и безопасности.
В то же время разработчики профессиональных аппаратов, наоборот, сосредотачивают свои усилия на усовершенствовании устройств и создании более контролируемых технологий, позволяющих получать ожидаемые и стабильные результаты. Например, Neogen PSR (Energist, Великобритания) является прямым «наследником» Portrait PSR, в котором доработаны технологии подачи импульсов.
Появляются устройства, в которых реализованы последние научные достижения в сфере использования плазмы. Среди них стоит выделить устройство Plasma BT(Seoulin Medicare, Корея), которое уже представлено на российском рынке. Это аппарат нового поколения, использующий не только уже хорошо известные тепловые эффекты плазменного воздействия, но и недавно открытые свойства холодной плазмы.
Plasma BT оснащен двумя отдельными насадками, которые генерируют плазму с различными характеристиками и, следовательно, разным влиянием на кожу (рис. 8).

Рис. 8. Аппарат Plasma BT
- Plasma Surgical — для термического воздействия, приводящего к сублимации ткани. Насадка позволяет поставлять плазму в виде одиночных импульсов или серии импульсов различной частоты, а также непрерывным потоком (рис. 9).
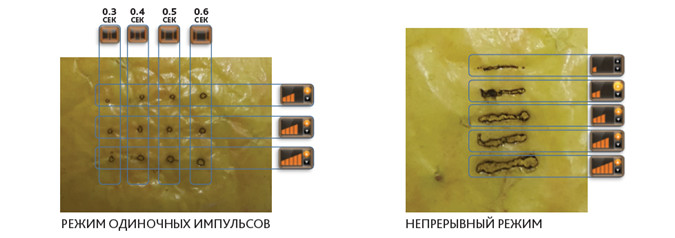
Рис. 9. Повреждения, генерируемые с помощью различных режимов насадки Plasma Surgical Plasma BT
При этом для каждого режима возможно изменить энергию, а следовательно — глубину и площадь воздействия.
Запатентованной разработкой Plasma BT является наличие специального направляющего фиксатора, который контролирует расстояние между иглой, испускающей плазму, и кожей (рис. 10).
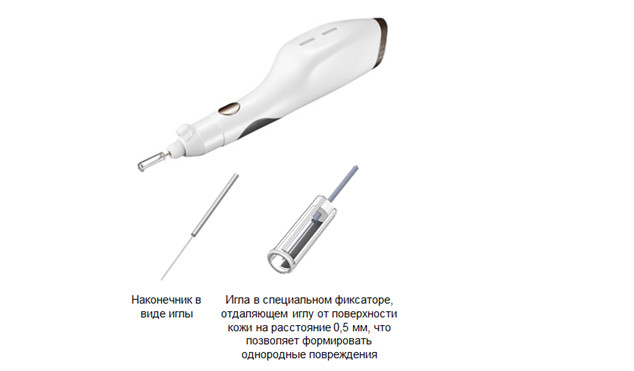
Рис. 10. Насадка Plasma Surgical Plasma BT с наконечником в виде иглы и иглой в специальном фиксаторе
Это позволяет производить обработку с оптимальной дистанции (0,5 мм) и формировать однородные повреждения по всей поверхности кожи. Используется для:
- подтяжки кожи (в том числе для так называемой безоперационной блефаропластики) (рис. 11) [16];
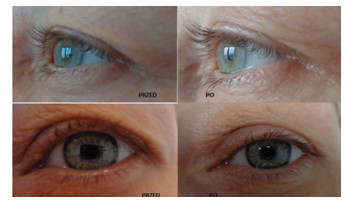
Рис. 11. Пациентка, 42 года, до (слева) и через 3 нед после блефаропластики с использованием устройства Plasma BT (импульсный режим, 40 Гц, уровень 2). Уменьшение размеров кожной складки открыло верхнее веко на 25% на правом глазу и на 46% на левом глазу, вследствие чего произошло расширение глазной щели на 14% для обоих глаз. Никаких серьезных побочных эффектов не возникало, отек разрешился через 2 дня, а мелкие струпья в точках повреждений отпали через 3 дня [по материалам доктора]
- устранения морщин;
- удаления пигментных пятен;
- устранения рубцов;
- удаления образований на коже.
- Plasma Poration (плазменный душ) — генерирует холодную плазму, которая обладает антибактериальными и противовоспалительными свойствами, а также стимулирует обновление клеток кожи и компонентов внеклеточного матрикса. Кроме того, отдельной сферой применения является увеличение трансдермальной доставки активных ингредиентов в кожу без ее повреждения (рис. 12).
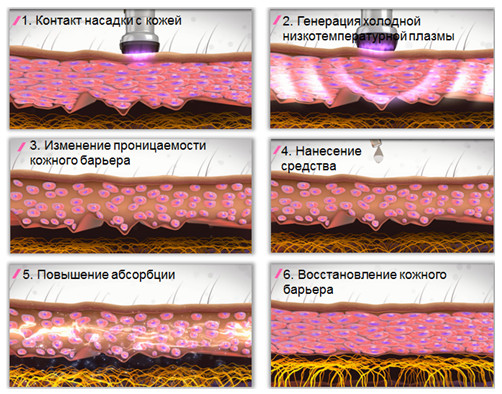
Рис. 12. Увеличение проницаемости кожного барьера с помощью плазменного душа
Используется для:
- омоложение кожи;
- лечения акне;
- улучшения проникновения различных активных веществ в кожу.
Показательный пример эффективности использования плазменного душа для трансдермальной доставки активных веществ приводится в статье доктора Беатрис Молина (Beatriz Molina) — медицинского директора и владелицы клиник Medlkas (Великобритания), ведущего специалиста Galderma UK [17]. Она описывает случай нарушения кровообращения при нехирургической ринопластике после введения филлера на основе гиалуроновой кислоты в кончик носа.
Поскольку инъекции гиалуронидазы были весьма болезненны для пациентки, доктор Молина использовала насадку Plasma Poration — 3 мин обработки кожи носа с последующим местным нанесением 1200 и 750 Ед гиалуронидазы в первые два дня после возникновения симптомов соответственно.
Вслед за этим она использовала насадку для трансдермального введения инъекционной формы гиалуроновой кислоты для биоревитализации (3 процедуры). Все нежелательные явления разрешились без каких-либо осложнений, что подтверждает эффективность использования плазменного душа для доставки в кожу крупных молекул (рис. 13).
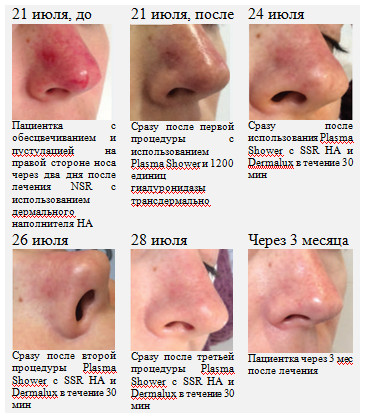
Рис. 13. Успешный опыт использования насадки Plasma Poration для трансдермального введения гиалуронидазы и гиалуроновой кислоты для биоревитализации
Заключение
Интерес к плазменным технологиям растет — это подтверждает большое количество устройств, которые появляются на рынке в последние годы. Плазменное омоложение обеспечивает более мягкое воздействие, чем аблятивные лазеры, однако сопровождается меньшим количеством нежелательных явлений и становится все более контролируемым. Дополнительным преимуществом является возможность использовать плазму для обработки темных фототипов кожи.
Кроме того, появились косметологические устройства, генерирующие холодную низкотемпературную плазму, что существенно расширяет перспективы использования плазменных технологий и позволяет предположить рост их популярности в будущем.
Литература
- Encyclopedia Britannica, britannica.com
- Kong M.G., Kroesen G., Morfill G. et al. Plasma medicine: an introductory review. New J Phys 2009: 11(115012); 1–35.
- Kos S., Blagus T., Cemazar M. et al. Safety aspects of atmospheric pressure helium plasma jet operation on skin: In vivo study on mouse skin. PLoS One 2017; 12(4): e0174966.
- Tiede R., Hirschberg J., Daeschlei G. et al. Plasma Applications: A Dermatological View. Contrib Plasma Phys 2014: 54(2); 118–130.
- Isbary G., Heinlin J., Shimizu T. et al. Successful and safe use of 2 min cold atmospheric argon plasma in chronic wounds: results of a randomized controlled trial. Br J Dermatol 2012; 167(2): 404–410.
- Lee O.J., Ju H.W., Khang G. et al. An experimental burn wound-healing study of non-thermal atmospheric pressure microplasma jet arrays. J Tissue Eng Regen Med 2016; 10(4): 348–357.
- Choi J.H., Song Y.S., Song K. et al. Skin renewal activity of non-thermal plasma through the activation of β-catenin in keratinocytes. Sci Rep. 2017 Jul 21; 7(1):
- Choi J.H., Lee H.W., Lee J.K. et al. Low-temperature atmospheric plasma increases the expression of anti-aging genes of skin cells without causing cellular damages. Arch Dermatol Res 2013; 305(2): 133–140.
- Shimizu K., Hayashida K., Blajan M. Novel method to improve transdermal drug delivery by atmospheric microplasma irradiation. Biointerphases 2015; 10(2): 029517.
- Graves D.B. Mechanisms of Plasma Medicine: Coupling Plasma Physics, Biochemistry and Biology. IEEE Transactions on Radiation and Plasma Medical Sciences 2017: 1(4); 281–292.
- Foster K.W., Moy R.L., Fincher E.F. Advances in plasma skin regeneration. J Cosmet Dermatol. 2008; 7(3): 169–179.
- Fitzpatrick R., Bernstein E., Iyer S. et al. A histopathologic evaluation of the Plasma Skin Regeneration System (PSR) versus a standard carbon dioxide resurfacing laser in an animal model. Lasers Surg Med 2008; 40(2): 93–99.
- Holcomb J.D., Kent K.J., Rousso D.E. Nitrogen plasma skin regeneration and aesthetic facial surgery: multicenter evaluation of concurrent treatment. Arch Facial Plast Surg 2009; 11(3): 184–193.
- Li X., Fang L., Huang L. In vivo histological evaluation of fractional ablative microplasma radio frequency technology using a roller tip: an animal study. Lasers Med Sci 2015; 30(9): 2287–2294.
- Zhang Z., Fei Y., Chen X. et al. Comparison of a fractional microplasma radio frequency technology and carbon dioxide fractional laser for the treatment of atrophic acne scars: a randomized split-face clinical study. Dermatol Surg 2013; 39(4): 559–566.
- Kaczyński K.J. The use of plasma in non-surgical blepharoplasty – a case study. Academy of Aesthetic and Anti-Aging Medicine 2017: 3; 2–6.
- Molina B. Case Study: Treating a NSR Complication. www.aestheticsjournal.com, 8 Dec 2017.
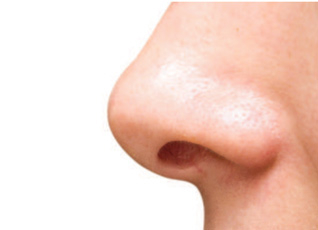
Большинство нехирургических методов, в которых дермальные наполнители с гиалуроновой кислотой (НА) используются для омоложения и / или устранения лицевой дисгармонии, обеспечивают безопасные, эффективные и воспроизводимые эстетические результаты. Дермальные наполнители НА позволяют корректировать глубокие морщины, складки и дефицит объема при возрастных изменениях или заболеваниях, их также можно использовать для внесения незначительных поправок после проведения хирургических процедур, таких как ринопластика1. Несмотря на благоприятный профиль безопасности наполнителей НА, могут возникать и побочные реакции. Большинство из них, как отмечают, являются умеренными и временными — серьезные побочные эффекты встречаются редко. Ранние побочные реакции на наполнители НА включают некроз и нарушения в сосудистой сетке, воспалительные реакции, связанные с инъекцией осложнения и неправильное размещение наполнителя. Среди отложенных реакций — узелки, гранулемы и обесцвечивание кожи. Большей части нежелательных явлений можно избежать; всестороннее понимание анатомии лица, подходящий выбор продукта для пациента и соответствующий метод асептики могут снизить вероятность их возникновения. При возникновении неблагоприятной реакции практикующие врачи должны иметь соответствующие знания и инструменты, доступные для эффективного лечения6.
Нехирургические ринопластические процедуры
«Нехирургическая ринопластика» (NSR) – это процедуры, в которых для формирования носа обычно используется дермальный наполнитель HA. Несмотря на то, что это относительно быстрая процедура, которая, как правило, занимает около 15-20 минут, ее следует выполнять только опытным практическим специалистам, поскольку нос представляет собой область с крайне высоким риском, так как имеет богатую кровеносную сеть3. Для успешного лечения врач, делающий инъекции, должен знать расположение соответствующих артерий. Лицевая артерия исходит из внешней сонной артерии и окружает нижнюю и переднюю границы нижней челюсти, расположенной перед жевательной мышцей. Она проникает в жевательную фасцию и поднимается наверх к глазу. Лицевая артерия лежит глубоко в скуловых мышцах и мимических, но не в щечной мышце и леваторе угла рта. На уровне рта лицевая артерия разветвляется на две губные артерии, нижнюю и верхнюю, в губы, где они проходят под круговой мышцей рта. Продолжение лицевой артерии вблизи медиального кантуса рядом с носом — угловая артерия4. В области носа наибольшей проблемой с точки зрения осложнений являются нарушения в сосудах и повреждение анатомической структуры. Если пациент проходил хирургическую ринопластическую процедуру и хочет немного улучшить этот результат с помощью дермального наполнителя, добавленные изменения анатомической изменчивости приводят к повышению риска возникновения нарушений сосудистого питания5.
Ситуационное исследование осложнений NSR
40-летняя пациентка, которая до этого проходила у меня три процедуры, пришла для прохождения еще одной процедуры NSR. До посещения моих процедур она перенесла хирургическую ринопластику, но все же имела небольшой послеоперационный дефект, который хотела исправить.
Пациентов, проходивших хирургические ринопластические операции, особенно трудно лечить, так как их система кровоснабжения может быть нарушена, поэтому практикующие врачи должны быть очень осторожны при использовании наполнителей7. 19 июля 2017 года я провела лечение NSR с использованием канюли 25G и дермального наполнителя НА. Небольшое количество лидокаина сначала вводили в кончик носа, затем иглу 23G использовали для облегчения точки входа канюли; важно отметить, что был вставлен только наконечник иглы. Я ввела 0,1 мл HA в кончик носа, затем 0.1 мл в правую часть. Во время процедуры я заметила, что небольшая область на правой части ее носа, куда вводился наполнитель, побелела (белое обесцвечивание). За 12 лет проведения сотен инъекций в нос, это был первый случай такой реакции. Я сразу же прекратила инъекцию, энергично промассировала область и наложила теплые компрессы. Через 30-40 секунд в коже был восстановлен кровоток и цвет стал нормальным. В течение процедуры пациентка не сообщала о боли или дискомфорте. Я решила прекратить процедуру и сообщила пациентке, что только что произошло. Выбор состоял в наблюдении за пациентом или использовании гиалуронидазы.
В некоторых исследованиях предполагается, что в случае такого осложнения практикующий врач должен немедленно использовать гиалуронидазу и массировать область, используя при этом теплые компрессы4,11. В них также утверждается, что гиалуронидазу следует вводить немедленно и ежедневно использовать в достаточных дозах, если присутствуют такие признаки и симптомы, как эритема, боль при инъекции или в последующие дни. Исследователи отмечают, что вы должны проводить процедуры в каждой области, где сосудистая система кажется нарушенной, а не только в области инъекции. Я объяснила ситуацию пациентке и обсудила с ней варианты; в частности, использование гиалуронидазы. Я рассуждала, следует ли вводить гиалуронидазу в этом случае, так как пациентка не испытывала никакой боли, и кожа имела нормальный окрас и хороший кровоток.
Мы договорились, что в течение 24 часов проведем контрольный прием, если не будет никаких изменений и проблем. Она прекрасно понимала, что может связаться со мной, если у нее возникнут какие-либо проблемы, и я дала ей свой личный номер мобильного телефона. Я посоветовала ей связаться со мной, если у нее возникнут какие-либо дискомфорт или боль, если на коже появится покраснение, я также показала ей фотографии кожи при нарушениях.
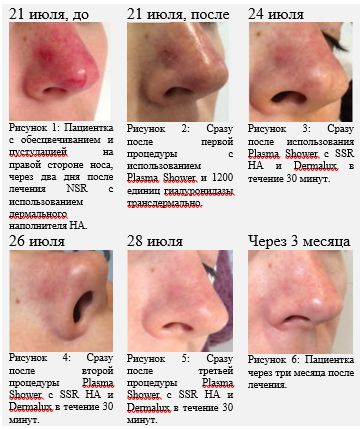
На этом этапе я попыталась придумать альтернативный способ введения гиалуронидазы, которая не требовала бы инъекций и, следовательно, не вызывала бы дополнительной боли у пациентки и не повреждала кровоснабжение носа еще больше. Я решила использовать устройство, в наличии в моей клинике, под названием Plasma Shower, часть платформы Plasma BT, в котором используется технология плазмы при атмосферном давлении. Раньше я использовала его в клинике, чтобы трансдермально вводить сыворотку в кожу без инъекций. Раньше я не использовала его для введения гиалуронидазы, но подумала, что могу воздействовать на НА путем трансдермального введения гиалуронидазы. Plasma Shower также описывается, как имеющий лечебные эффекты13,14, которые, как я думала, станут дополнительным преимуществом. Я начала с использования Plasma Shower на носу в течение трех минут. Затем я местно наложила 0,2 мл гиалуронидазы на нос. При внутрисосудистом инфаркте рекомендуют использовать минимум 200-300 единиц гиалуронидазы (распространяются по всей площади надвигающегося некроза), процедуры повторяются ежедневно в течение минимум двух дней, пока не появятся признаки постоянного некроза или восстановленного кровотока. При необходимости предлагаются дозы до 1500 единиц, потому что следствием недостаточной дозировки является некроз тканей. Также рекомендуют проводить приемы пациента каждые 24 часа4. В других рекомендациях предлагается минимум 500-600 единиц6. Поэтому я рассмотрела эти рекомендации по местному использованию гиалуронидазы. Следовательно, я нанесла 600 единиц гиалуронидазы местно на нос (1500 ед. ампула, разведенная в 10 мл хлорида натрия). Я заметила улучшение, но оно было слишком медленным, поэтому приняла решение повысить концентрацию для улучшения его эффективности. Я решила разбавить 1 500 единиц гиалуронидазы в 1 мл хлорида натрия и наложила еще 600 единиц. В общей сложности 1200 единиц гиалуронидазы вводили трансдермально. К моему большому облегчению, пациентка почувствовала, что боль утихла, и мы заметили, что цвет кожи резко улучшался (Рисунок 2). Как только пациентке стало комфортно, боли при пальпации не было, я прекратила процедуру и договорилась встретиться с ней на следующий день, чтобы посмотреть результаты. Когда она вернулась 22 июля, пациентка чувствовала себя лучше, чем в предыдущий день, но на кончике носа оставалась некоторая легкая чувствительность. Я решила повторить процедуру, пока пациентка не чувствовала боль. Я ввела еще 750 единиц гиалуронидазы трансдермально.
Мы договорились поговорить следующим утром, чтобы обсудить возможность дальнейшего лечения гиалуронидазой. Когда я позвонила ей в воскресенье утром 23 июля, пациентка сказала, что чувствует значительное улучшение, у нее не было никакой боли и ей не хотелось приходить на прием. Мы договорились отложить осмотр до понедельника. В понедельник, 24 июля, пациентка вернулась в мою клинику. Она не испытывала боли, и цвет кожи казался намного лучше, но я решила попробовать помочь коже зажить и восстановиться увлажнением и стимуляцией регенерации. Я снова использовала устройство Plasma Shower, чтобы ввести продукт НА, гидратировать клетки и ускорить восстановление. Я решила использовать SSR HA Injectable, потому что использовала его в клинике, чтобы способствовать восстановлению кожи после глубокого химического пилинга. Затем мы продолжили лечить пациентку под светодиодным фототерапевтическим устройством (Dermalux) в течение 30 минут, чтобы решить проблему покраснения (Рисунок 4). Мы повторили эту же процедуру в среду 26 июля (Рисунок 5) 3 и в пятницу 28 июля, чтобы интенсивнее помочь коже восстанавливаться и увлажнить ее4 (Рисунок 6)5.
Обсуждение
Важно, чтобы практикующие врачи имели возможность распознавать осложнения и принимать правильные клинические решения для успешного лечения. Хотя пациентка была явно обеспокоена осложнениями, она приходила ко мне на лечение в течение многих лет и доверяла моему клиническому суждению. Я обеспечила возможность связаться со мной в любое время, пока мы справлялись с этим осложнением, и после прохождения первой процедуры она была очень довольна результатом. С тех пор мы не вводили инъекций в нос, но она должна была посетить меня для проведения других процедур. Я бы никогда не подумала о повторной инъекции в эту зону в течение как минимум трех-четырех месяцев, в идеале шести. Доказательств или статей, подтверждающих это утверждение, нет; однако мне кажется, что при лечении пациентов с известными осложнениями идея действовать осторожно является здравой. Другим практикующим врачам, которые сталкиваются с подобными осложнениями, когда им кажется, что инъекция гиалуронидазы может вызвать дальнейшую боль, дискомфорт и раздражение, я хотела бы сказать, что введение гиалуронидазы трансдермально является полезным решением. Я считаю, что такой подход к осложнениям чрезвычайно интересен и будет полезен для дальнейшего изучения. Поэтому я в настоящее время провожу ретроспективное исследование, чтобы изучить процедуру, после чего я надеюсь разработать протокол для ее использования.

Плазма – это четвертое агрегатное состояние вещества, которое существует в естественных условиях в определенных ситуациях (плазмой является солнце или молния во время грозы) [1]. Плазма была открыта уже в девятнадцатом веке. Ее изучали, в частности, Эрнст Вернер фон Сименс и Майкл Фарадей [2]. Плазма нашла широкое применение в 20-м веке, она используется в уличном освещении, искра, создаваемая свечой зажигания, – это тоже плазма [1]. В медицине ее начали использовать около двадцати лет тому назад, в основном из-за ее разрушительных свойств (например, в электрохирургии) [3].
Только недавно стали использовать стимулирующее воздействие плазмы на живые ткани и клетки. Применение плазмы в приложении непосредственно к человеческому телу требовало поддержания ее температуры на уровне ниже 40° С, чтобы предотвратить опасность термических повреждений [4].
Такие условия гарантируются плазмой атмосферного давления (cold atmospheric pressure plasma), которая возникает в результате воздействия электрической энергии на биологически неактивный газ, такой как аргон, азот, гелий или воздух. Практически вся электрическая энергия расходуется на возбуждение электронов, в то время как атомы, ионы и частички газа, оставаясь в низковозбужденном состоянии, воздействуют на другие молекулы атмосферного воздуха. Как следствие, это приводит к созданию плазмы, обладающей биологическим потенциалом [4]. Медицинскую плазму, или холодную плазму – как ее часто называют – нередко сравнивают с молнией. Это не вполне точное сравнение, поскольку из-за высокой энергии (высокой плотности электронов) плазма, создающая молнию, обладает разрушительными свойствами в очень высокой степени [5].
Имеющиеся в настоящее время в Европе аппараты используют для создания плазмы постоянный ток (например, электрическую дугу), переменный ток (например, разряд с диэлектрическим барьером), радиоволны, микроволны или плазменные потоки [6]. Плазма может быть произведена, в частности прямым или косвенным способом. В случае непосредственно генерируемой плазмы разрядный промежуток находится между электродом устройства и телом пациента. При приближении электрода устройства на расстояние около 0,5-1 мм наблюдается микроволновое излучение и генерация плазмы [7, 8].
Рисунок 1. Аппарат «Plasma BT» («Плазма БT»)
Работа прибора «Plasma BT» основывается на применении технологии F-DBD (плавающий диэлектрический барьерный разряд), защищенной четырьмя патентами, где используется естественный способ получения плазмы (из кислорода и азота, содержащихся в воздухе) на основе переменного тока [9], создавая низкотемпературную плазму (температура не превышает 40° C), которая в небольшой степени ионизирована и имеет высокое содержание нейтральных частиц [4].Аппарат «Plasma BT» (рис. 1) сертификат CE номер IT271142..

Рисунок 2. Запатентованная игла с фиксатором
Аппарат имеет 3 режима работы (Shot, Pulse, Continuous) и 5 уровней регулирования выходной мощности.
При работе с данным аппаратом не требуется заземление для защиты пациента [10]. В аппарате «Plasma BT» используется запатентованная игла с фиксатором (рис. 2), которая позволяет фиксировать устройство непосредственно на теле пациента, что улучшает точность лечения и скорость заживления.
Практические аспекты проведения блефаропластики верхнего века без хирургического вмешательства с использованием аппарата «Plasma BT»
Специалист, выполняющий эту процедуру, должен знать топографию периорбитальной области [11] с учетом антропологических различий. Например, существует 4 варианта европеоидного окаймления глаз [13]. Врач также должен обладать умением отличить птоз (опущение верхнего века) от его кажущегося опущения в процессе дерматохалазиса [12].
Прежде чем приступать к процедуре, следует обсудить с пациентом ход процедуры и течение процесса заживления, а также получить письменное согласие на процедуру. Также необходимо предупредить пациента о необходимости проведения нескольких процедур в случае большого избытка кожных складок в области век и подготовить его к отсутствию улучшения или даже к незначительному увеличению нависания кожи в случае дерматохалазиса с сопутствующим отеком век.
На рис. 4 и 5 представлены результаты лечения 42-летней женщины (контрольные снимки были сделаны через 3 недели после процедуры) с использованием аппарата «Plasma BT» со следующими настройками: Pulse, 40Hz, Level 2.
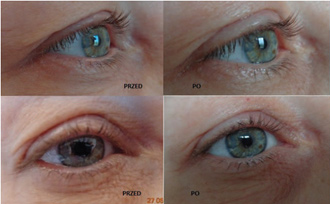
Рис. 4 Правое веко: до и через 3 недели после первой процедуры.
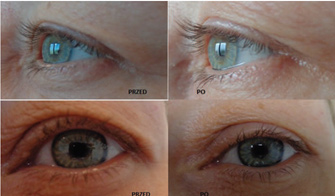
Рис. 5. Правое веко: до и через 3 недели после первой процедуры.
Пациентка оценила результат первой процедуры на 3 (видимое улучшение) по 5-балльной шкале GAIS (Шкала общего эстетического улучшения) и была удовлетворена процессом заживления (отек уменьшился через 2 дня, а мелкие струпья на точках сублимации отпали через 3 дня). Была сделана коррекция избыточной кожи и была уменьшена асимметрия, имевшаяся между двумя веками до процедуры. Уменьшение складки века открыло верхнее веко на 25% на правом глазу и на 46% на левом глазу, вследствие чего произошло расширение глазной щели на 14% для обоих глаз.
Резюме
Избыток кожи в складках век, появляющийся с возрастом, является серьезной эстетической проблемой. До недавнего времени единственным доступным методом лечения было хирургическое удаление избыточной кожи. С некоторого времени стал доступен альтернативный метод, заключающийся в использовании так называемой холодной плазмы.
С января этого года в Европе появился новый аппарат Plasma BT (сертификат CE номер IT271142) с использованием технологии F-DBD, защищенный четырьмя патентами, включая запатентованную иглу с фиксатором.
«Plasma BT» – это универсальный аппарат, который будет отвечать ожиданиям как тех врачей, которые начинают «свою практику» с холодной плазмой, так и тех, которые ожидают от аппарата возможности индивидуализировать терапию путем адаптации настроек аппарата к клинической ситуации, что не давали плазменные аппараты предыдущего поколения.
Насадка с фиксатором позволяет проводить точную сублимацию в точках воздействия, что может облегчить выполнение первых процедур, кроме того, ее охотно будут использовать эксперты, которые оценят удобство и, прежде всего, скорость работы с насадкой и, как следствие, более короткое время заживления. Для приверженцев традиционных методов с «твердой рукой» в комплектации прибора имеется также классическая хирургическая игла без фиксатора, которая используется в том числе для удаления новообразований.
Аппарат «Plasma BT» дает оператору возможность выбирать 5 уровней мощности, доступных в трех режимах работы (shot, pulse и continuous). Режим «shot» позволяет точно определить время генерации плазмы прибором в диапазоне 0,3 –0,6 с; лица, имеющие опыт работы с прибором, оценят режим «pulse» (например, при большой площади обработки) и «continuous» (например, при удалении новообразований).
В клиническом случае, представленном в данной публикации, аппарат «Plasma BT» оказался эффективным и безопасным устройством, дающим возможность улучшить качество жизни пациента (избыток складки века начал покрывать ресницы на верхнем левом веке и сужать глазную щель) без необходимости хирургического вмешательства.
Пациентка, подвергшаяся процедуре, оценила быстрое время заживления (отек век, характерный для данной процедуры, и мелкие струпья в точках сублимации оставались не более 3 дней) и не сообщала о серьезных побочных эффектах, кроме типичных, таких как: чувство тепла в области века сразу после обработки, небольшое слезотечение, наблюдавшееся в первый день, покраснение век, сохранявшееся до 7 дней после процедуры.
«Plasma BT» является эффективной альтернативой хирургической блефаропластике при лечении избыточной складки века, что дает возможность индивидуализации терапии благодаря 5 уровням мощности и 3 режимам работы. Использование запатентованной насадки для хирургической иглы делает более удобной работу оператора и обеспечивает точность процедуры, сокращает время процедуры и, прежде всего, время заживления.

Д-р Кшиштоф Яцек Качиньски
является выпускником медицинского факультета Медицинской академии в Гданьске, Курс фармакоэкономики, маркетинга и фармацевтического права (окончил с очень хорошим результатом). С отличием окончил аспирантуру Школы эстетической медицины Польского медицинского общества, работающей совместно с Международной ассоциацией эстетической медицины (UIME) в Париже, получив звание врача эстетической медицины.
Член Польского общества эстетической медицины и борьбы с возрастом (Anti-Aging).
